Apa yang terjadi jika suatu larutan elektrolit dialiri arus listrik searah? larutan elektrolit akan terionisasi menjadi ion positif dan ion negatif. Apabila dialiri arus listrik, ion-ion dari larutan akan bergerak menuju ke kutub listrik yang berlawanan muatan. Ion-ion negatif akan bergerak ke kutub positif dan ion-ion positif akan bergerak ke kutub negatif.
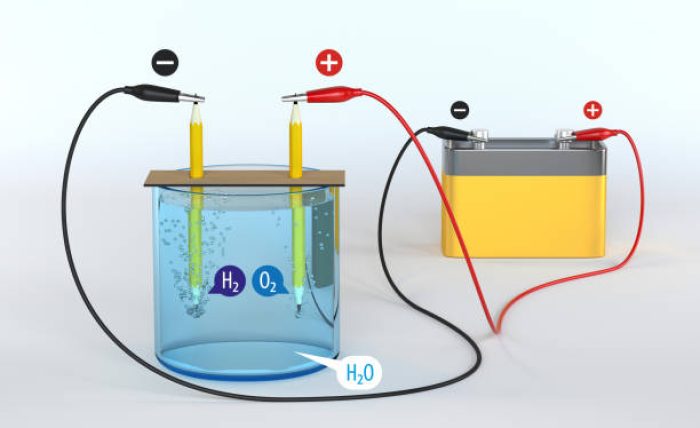
Sel elektrolisis merupakan kebalikan dari sel Volta dimana listrik digunakan untuk melangsungkan reaksi redoks tidak spontan. Susunan sel elektrolisis dapat dilihat pada Gambar di bawah ini.

Sumber gambar: https://akupintar.id/info-pintar/-/blogs/sel-elektrolisis-pengertian-proses-reaksi-dan-contohnya
Sel elektrolisis terdiri dari sebuah wadah, elektroda, elektrolit dan sumber arus searah. Pada peristiwa elektrolisis, elektroda positif bertindak sebagai anoda dan elektroda negatif sebagai katoda. Hasil reaksi elektrolisis dipengaruhi oleh zat yang dielektrolisis (leburan atau larutan) dan elektroda. Elektroda yang tidak ikut bereaksi (inert) adalah C (grafit), Pt, dan Au sedangkan yang lain merupakan elektroda tidak inert (ikut bereaksi).
Zat yang dielektrolisis
1) Zat murni / leburan elektrolit: ion-ion di katoda akan direduksi dan ion-ion di anoda langsung teroksidasi
2) Larutan: ketentuan reaksi di anoda dan katoda dijelaskan lebih lanjut pada link materi di bawah ini.
Stoikiometri Reaksi Elektrolisis
Hukum Faraday I
Michael Faraday telah menemukan hubungan kuantitatif antara massa zat yang dibebaskan pada elektrolisis berbanding lurus dengan jumlah listrik yang digunakan.
Hukum Faraday 2
“Massa zat yang dibebaskan pada elektrolisis berbanding lurus dengan massa ekuivalen zat tersebut”
Penerapan elektrolisis pada proses industri salah satunya adalah industri logam. Indonesia merupakan salah satu negara penghasil tambang logam seperti nikel, tembaga, emas dan yang lainnya. Hasil tambang adalah bijih logam dimana harus diolah terlebih dahulu menjadi logam melalui reaksi elektrolisis. Selain itu, elektrolisis digunakan juga pada proses produksi zat seperti logam-logam alkali, magnesium, aluminium serta penyepuhan.
Penjelasan materi lebih lanjut silahkan KLIK LINK MATERI di bawah ini.
https://drive.google.com/file/d/1uJlOikObIr7AKd148BH0qQkiDPs6IbMG/view?usp=sharing