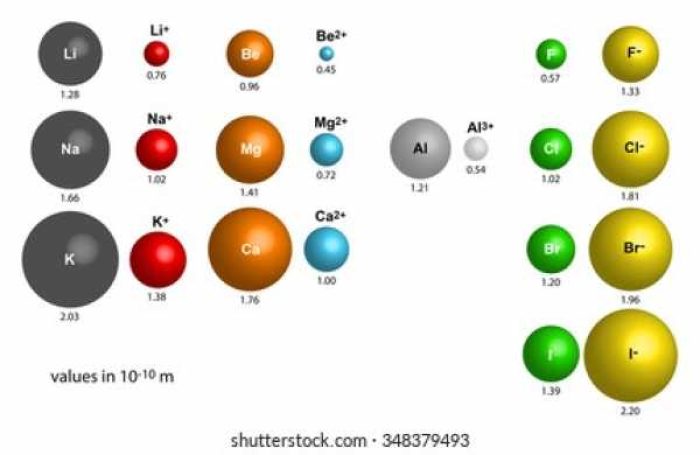
Anak-anak kalian sudah mempelajari tentang hubungan konfigurasi elektron dengan letak unsur dalam tabel periodik, perkembangan pengelompokan unsur terakhir yang akan kita pelajari sekarang ini adalah sifat-sifat periodik unsur.
Sifat periodik merupakan sifat yang berubah secara beraturan sesuai dengan kenaikan nomor atom yaitu dari kiri ke kanan dalam satu periode atau dari atas ke bawah dalam satu golongan. Sifat-sifat periodik yang akan dibahas adalah jari-jari atom, jari-jari ion, energi ionisasi, afinitas elektron, keelektronegatifan, sifat logam dan non logam, kereaktifan serta titik leleh dan titik didih. Sifat-sifat unsur tersebut erat hubungannya dengan konfigurasi elektron sehingga berhubungan langsung dengan periode dan golongan. Dalam satu golongan atau periode yang sama sifat-sifat tersebut mempunyai keteraturan tertentu.
Jari-jari atom merupakan jarak dari inti atom hingga kulit elektron terluar. Energi ionisasi adalah energi yang diperlukan untuk melepas satu elektron terluarnya. Energi yang menyertai penambahan satu elektron pada suatu atom netral dalam wujud gas membentuk ion bermuatan -1 yang disebut dengan afinitas elektron.
Untuk sifat-sifat yang lain silahkan kalian klik LINK MATERI berikut ini.
LINK MATERI: https://drive.google.com/file/d/1vWt7b9PKqT1WXdIYnDtkNJAy6lxcU3ZG/view?usp=sharing