Apakah kalian tahu apa yang dimaksud reaksi redoks? reaksi redoks merupakan reaksi yang terdiri dari reaksi reduksi dan oksidasi. Reaksi redoks banyak terjadi di dalam kehidupan sehari-hari seperti reaksi pembakaran, perkaratan besi, peristiwa pemecahan glukosa di dalam tubuh. Selain itu, dimanfaatkan dalam teknologi dan industri misalnya baterai pada mobil listrik dan handphone.
Tujuan pembelajaran pada materi ini sebagai berikut:
1.Menyetarakan persamaan reaksi redoks dengan cara bilangan oksidasi dan cara setengah reaksi.
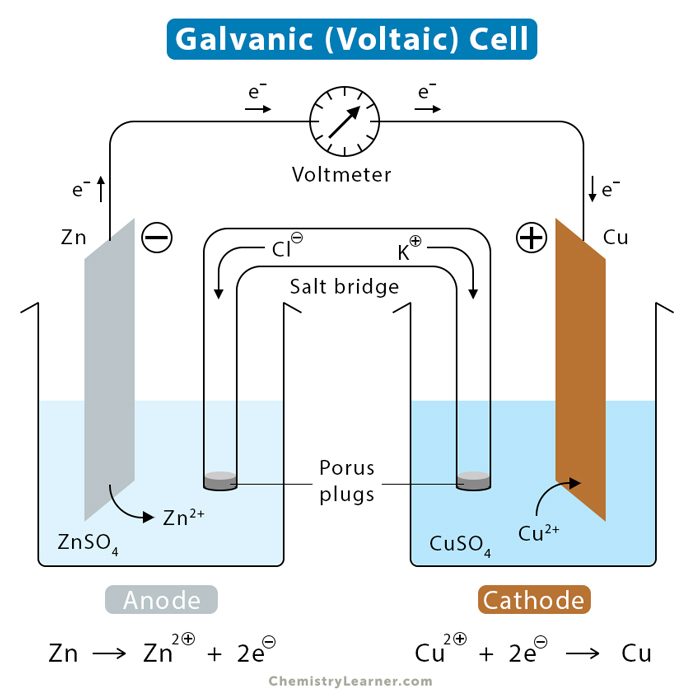
2.Mendeskripsikan bagian-bagian dari sel volta (anode, katode, reaksi sel, beda potensial, dan notasi sel) melalui diskusi kelompok dan literasi.
3.Mendeskripsikan potensial elektrode, elektrode standar, dan potensial elektrode standar serta cara pengukurannya melalui diskusi kelompok dan literasi.
4.Menganalisis hasil percobaan untuk mendeskripsikan hubungan antara potensial elektrode dengan kekuatan/daya reduksi dan daya oksidasi suatu zat.
Sebelum itu, kita review kembali terkait perkembangan konsep redoks.
A. Konsep Redoks
1.Konsep perpindahan oksigen
- Reduksi: reaksi pelepasan oksigen dari suatu senyawa
- Oksidasi : reaksi pengikatan (penggabungan) oksigen oleh suatu zat
2.Konsep perpindahan elektron
- Reduksi: reaksi pengikatan elektron
- Oksidasi: reaksi pelepasan elektron
3.Konsep perubahan bilangan oksidasi
Bilangan oksidasi merupakan bilangan yang diberikan kepada suatu unsur di dalam membentuk senyawa atau ion.
- Reduksi: reaksi penurunan bilangan oksidasi
- Oksidasi: reaksi pertambahan bilangan oksidasi
B.Penyetaraan Persamaan Reaksi Redoks
1. Cara setengah reaksi
Penyetaraan persamaan reaksi redoks dengan cara setengah reaksi, yaitu dengan melihat elektron yang diterima atau dilepaskan. Penyetaraan dilakukan dengan menyamakan jumlah elektronnya. Cara ini diutamakan untuk reaksi dengan suasana reaksi telah diketahui.
2.Cara perubahan bilangan oksidasi
Penyetaraan persamaan reaksi dengan cara perubahan bilangan oksidasi, yaitu dengan cara melihat perubahan bilangan oksidasinya.
C.Sel Volta
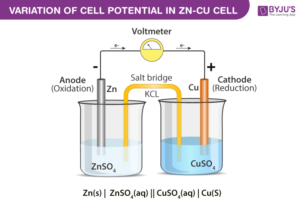
Sel volta merupakan sel yang menggunakan reaksi redoks spontan untuk menghasilkan arus listrik. Elektroda tempat terjadinya reaksi oksidasi disebut anoda sedangkan elektroda tempat terjadinya reaksi reduksi disebut katoda. Katoda bermuatan positif dan anoda bermuatan negatif.
Pemahaman materi lebih lanjut silahkan klik LINK MATERI di bawah ini.
https://drive.google.com/file/d/1dRlMug34nA77nxyrBe1WZ6b_Ni-r_2Dn/view?usp=sharing